Επιμερές
Στην στερεοχημεία, ως επιμερές ορίζεται κάθε ένωση από ένα ζεύγος διαστερεομερών.[1] Τα δύο επιμερή έχουν αντίθετη διαμόρφωση μόνο σε ένα στερεογονικό κέντρο από τα τουλάχιστον δύο.[2] Όλα τα υπόλοιπα στερεογονικά κέντρα στις ενώσεις αυτές είναι όμοια. Επιμερισμός - συνεπώς - είναι η αλληλομετατροπή του ενός επιμερούς στο άλλο επιμερές του.
Η δοξορουβικίνη και η επιρουβικίνη είναι δύο επιμερή που χρησιμοποιούνται ως φαρμακευτικές ουσίες.

|
| Σύγκριση επιμερών - δοξορουβικίνης & επιρουβικίνης |
Παραδείγματα[Επεξεργασία | επεξεργασία κώδικα]
Τα στερεοϊσομερή β-D-γλυκοπυρανόζη και β-D-μαννοπυρανόζη είναι επιμερή διότι διαφέρουν μόνο στη στερεοχημεία τους, ήτοι στη θέση του άνθρακα, C-2.
Η υδροξυλική ομάδα στη β-D-γλυκοπυρανόζη είναι ισημερινή (στο «επίπεδο» του δακτυλίου), ενώ στη β-D-μαννοπυρανόζη η υδροξυλική ομάδα στο C-2 είναι αξονική (πάνω από το «επίπεδο» του δακτυλίου). Αυτά τα δύο μόρια είναι επιμερή αλλά, επειδή δεν είναι κατοπτρικά είδωλα το ένα του άλλου, δεν είναι εναντιομερή. Τα εναντιομερή έχουν την ίδια ονομασία, αλλά διαφέρουν στην ταξινόμηση D και L. Επίσης δεν είναι ανωμερή σακχάρου, αφού δεν είναι ο ανωμερής άνθρακας που εμπλέκεται στη στερεοχημεία.
Παρομοίως, η β-D-γλυκοπυρανόζη και η β-D-γαλακτοπυρανόζη είναι επιμερή, τα οποία διαφέρουν στη θέση του άνθρακα C-4, αφού στην πρώτη ένωση είναι ισημερινό (το υδροξύλιο -ΟΗ) και στην δεύτερη είναι αξονικό.

|

|
| β-D-γλυκοπυρανόζη | β-D-μαννοπυρανόζη |
Στην περίπτωση εκείνη που η διαφοροποίηση υφίσταται στο -ΟΗ στην ανθρακική θέση C-1, ο ανωμερής άνθρακας, όπως στην περίπτωση της α-D-γλυκοπυρανόζης και της β-D-γλυκοπυρανόζης, τα μόρια είναι και επιμερή και ανωμερή (όπως υποδεικνύεται από τον χαρακτηρισμό -α και -β).[3]

|

|
| α-D-γλυκοπυρανόζη | β-D-γλυκοπυρανόζη |
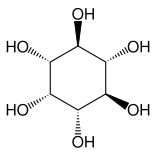
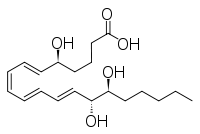
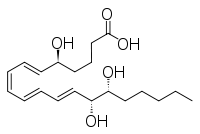
Άλλες στενά συγγενείς ενώσεις είναι η επι-ινοσιτόλη και η ινοσιτόλη, όπως και η λιποξίνη και η επιλιποξίνη.

|
|
|
|
επι-ινοσιτόλη
|
ινοσιτόλη
|
λιποξίνη
|
επιλιποξίνη
|
Επιμερισμός[Επεξεργασία | επεξεργασία κώδικα]
Ο επιμερισμός είναι χημική διαδικασία όπου ένα επιμερές μετατρέπεται στο διαστερεομερικό αντίστοιχό του.[1] Μπορεί αυτό να συμβεί μέσα από αντιδράσεις αποπολυμερισμού συμπυκνωμένων τανινών. Ο επιμερισμός μπορεί να είναι αυθόρμητος (αργή διαδικασία) ή να καταλυθεί από ένζυμα.
Το προτελευταίο βήμα στην κλασική σύνθεση επιμπατιδίνης - των Zhang & Trudell - αποτελεί κλασικό παράδειγμα επιμερισμού.[4] Άλλα φαρμακευτικά παραδείγματα περιλαμβάνουν τον επιμερισμό των ερυθροϊσομερών της μεθυλφαινιδάτης προς τα φαρμακολογικά προτιμώμενα και χαμηλότερης ενέργειας θρεο-ισομερή, και στον ανεπιθύμητο in vivo επιμερισμό της τεσοφενσίνης σε μπραζοφενσίνη.
Παραπομπές[Επεξεργασία | επεξεργασία κώδικα]
- ↑ 1,0 1,1 Clayden, Jonathan· Greeves, Nick (2012). Organic Chemistry (2nd έκδοση). Oxford University Press. σελ. 1112.
- ↑ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997). Online corrected version: (2006–) "Epimers".
- ↑ Structure of the glucose molecule
- ↑ Zhang, Chunming; Trudell, Mark L. (1996). «A Short and Efficient Total Synthesis of (±)-Epibatidine». The Journal of Organic Chemistry 61 (20): 7189–7191. doi:. ISSN 0022-3263. PMID 11667626.
